Во
время учебы в ЛЭТИ познакомился с титанатом бария, который в
зависимости от условий может менять кристаллическую структуру до четырех
разных модификаций. С тех пор и пытаюсь обьяснить механизм этих фазовых
переходов. А попутно исследую и другие свойства химических элементов.
Чтобы досконально разобраться, наверное, необходимо классифицировать
элементы, понять их распределение в таблице элементов. Рассмотреть все
варианты возможных размещений в атоме и ядре протонов, нейтронов и
электронов. Что и сделано в предлагаемой работе.
Модель ядра атома и таблица элементов.
Капельная модель
Была предложена Нильсом Бором в 1936 году в рамках теории составного ядра[1]. Согласно этой теории, атомное ядро можно представить в виде сферической равномерно заряженной капли из особой ядерной материи, которая обладает несжимаемостью, насыщением ядерных сил, «испарением» нуклонов (нейтронов и протонов), напоминая жидкость. Эта модель развивалась Яковом Френкелем и, в дальнейшем, Джоном Уилером, на её основании Карлом Вайцзеккером была получена полуэмпирическая формула для энергии связи ядра атома, названная в его честь формулой Вайцзеккера. Капельная модель является макроскопической теорией, она не учитывает микроскопического строения ядра, например, распределения ядерных оболочек.Модель хорошо описывает важнейшие свойства ядер — свойство насыщения, т.е. пропорциональность энергии связи тяжёлых ядер массовому числу A = N+Z; зависимость радиуса ядра R от A:
Оболочечная модель
Предложена в 1932 году Дмитрием Иваненко совместно с Евгением Гапоном, в 1949 году дополнена Марией Гёпперт-Майер и Хансом Йенсеном. Аналогична теории оболочечного строения атома, в которой электроны наполняют электронные оболочки, и, как только оболочка заполнена, значительно понижается энергия связи для следующего электрона. Согласно модели ядро представляет собой систему нуклонов, независимо движущихся в усреднённом поле, создаваемом силовым воздействием остальных нуклонов. Каждый нуклон находится в определённом индивидуальном квантовом состоянии, характеризуемом энергией, моментом вращения j, его проекцией m на одну из координатных осей и орбитальным моментом вращения l = j± 1/2. Энергия уровня не зависит от проекции момента вращения на внешнюю ось, поэтому на каждом энергетическом уровне с моментами j, l может находиться (2j + 1) нуклонов, образующих оболочку (j, l). Совокупность близких по энергии уровней образует оболочку ядра. Когда количество протонов или нейтронов достигает магического числа, отвечающего заполнению очередной оболочки, возникает возможность скачкообразного изменения некоторых характеризующих ядро величин (в частности, энергии связи). Физической причиной периодичности является принцип Паули, запрещающий двум тождественным фермионам находиться в одном и том же состоянии.Оболочечная модель позволила объяснить спины и магнитные моменты ядер, различную устойчивость атомных ядер, а также периодичность изменений их свойств, применима для описания легких и средних ядер, а также ядер, находящихся в основном состоянии[4].
Модель не объясняет деформированные ядра.
Коллективная модель ядра
Предложена в 1952 году Оге Бором и Б. Моттельсоном. Возникла на основе капельной модели. Рассматривает ядро как остов, образованный нуклонами заполненных оболочек и внешних нуклонов, движущихся в поле создаваемом нуклонами остова. Модель объяснила природу низколежащих возбуждений ядер, которые интерпретируются как динамическая деформация поверхности.Обобщённая модель ядра
Предложена в 1952 году Оге Бором и Б. Моттельсоном. Объяснила большие квадрупольные моменты некоторых ядер тем, что внешние нуклоны таких ядер деформируют остов, который становится вытянутым или сплюснутым.Ротационная модель
Согласно экспериментальным данным в области массовых чисел 150 < A < 190 и А > 200, квадрупольные моменты ядер чрезвычайно велики и отличаются от значений, предсказываемых оболочечной моделью, в десятки раз. В этой же области значений А зависимость энергии нижних возбуждённых состояний ядер от спина ядра оказывается похожей на зависимость энергии вращающегося волчка от его момента вращения. Согласно модели ядро предполагается несферическим.Существенная черта ротационной модели — сочетание вращения всего ядра, как целого, с движением отдельных нуклонов в несферическом потенциальном поле. При этом предполагается, что вращение всего ядра происходит достаточно медленно по сравнению со скоростью движения нуклонов. Ротационная модель позволяет описать ряд существенных свойств большой группы ядер, при этом необъяснённым остаётся сам факт возникновения ротационного спектра (факт вращения всего ядра, как целого).
Модель ядра атома, предложенная нами и таблица элементов.
Каждый последующий химический элемент отличается
от предыдущего тем, что в его ядре количество протонов
увеличивается на единицу, а количество нейтронов растет, в
общем случае, на несколько. В статье предлагается модель ядра
атома, объясняющая это явление.
То есть в ядре всегда больше нейтронов, чем
протонов (не считая самых легких ядер). В литературе это странное
соотношение числа нейтронов к числу протонов для любого ядра
ничем не объясняется.
Для построения модели ядра атома отметим, что при альфа-
радиоактивности ядра гелия имеют примерно равные энергии.
Поэтому на внешней оболочке ядра разместим все протоны с таким
же количеством нейтронов. При этом на одном энергетическом
уровне смогут находиться только бозоны, какими размещенные на
внешней оболочке ядра альфа-частицы и являются. Внутри ядра
расположим оставшиеся нейтроны, задачей которых будет
ослабление электростатических полей отталкивания протонов.
Предположив ядро сферическим, а радиусы протона и нейтрона
примерно одинаковыми, для любого элемента получим модель ядра,
объясняющую отношение числа нейтронов к числу протонов,
вытекающее из упаковки ядра атома нуклонами.
Если массу ядра принять первичной, а химические свойства атома
вторичными, то в таблице элементов атомный вес должен
монотонно изменяться как по горизонтали, так и по вертикали.
Доклады независимых авторов 2005 выпуск №1
173
Построив таблицу по этим признакам, мы вынуждены будем после
лютеция и лоуренсия оставить по четыре пустых места, чтобы
таблица отражала химические свойства элементов - см. табл. 1.
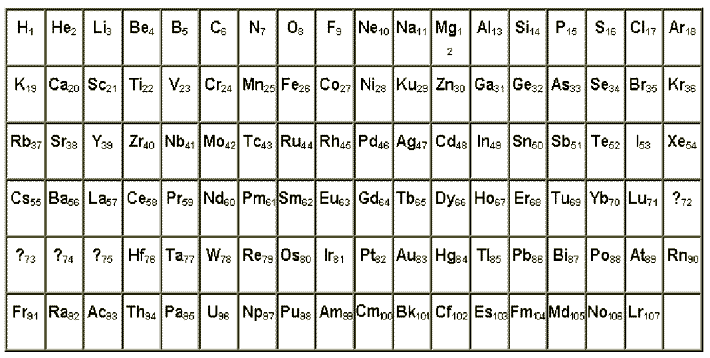
В таблице заполнены все ячейки. У Д.И.Менделеева не таблица, а сложная конструкция. Лантаноиды и актиноиды, которые должны располагаться вертикально согласно их химических свойств, по "домашнему" расположены под таблицей горизонтально.
Антониус Йоханнес ван ден Брук (нидерл. Antonius Johannes van den Broek; 4 мая 1870, Зутермер — 25 октября 1926, Билтховен (нид.)русск.) — нидерландский юрист и физик-любитель. Несмотря на отсутствие специального образования, получил несколько результатов, оставивших след в истории науки. Ему принадлежит первая формулировка положения о равенстве порядкового номера элемента в периодической системе заряду атомного ядра. С именем ван ден Брука связано возникновение ранних теоретических представлений о составе ядра, в частности им была предложена протон-электронная модель ядерного строения. В своих работах он неоднократно пытался найти верный принцип расположения элементов в периодической системе и разработать метод вычисления всех возможных в природе изотопов.
Согласно этой таблице элементов построенной, как по закону Менделеева, а также по правилу ван-Брука, начиная с гафния заряды ядер могут быть на 4 единицы больше, чем принято на сегодня при той же массе.
Построив таблицу, мы вынуждены были после
лютеция и лоуренсия оставить по четыре пустых места, чтобы
таблица отражала химические свойства элементов.
Наверное Джеймс Чедвик сделал ошибку, измеряя заряды ядер атомов.
Точнее не ошибку в измерениях, а в том что согласился с таблицей Менделеева и полученный результат для платины 77,6 был трактован, как заряд ядра равный 78, согласно таблице.
Для меди был получен результат 29,3- больше истинного на 0,3, для серебра 46,3 уже меньше истинного на 0,7, а для платины меньше "истинного" всего на 0,6. Уменьшение связано с экранированием протонов друг другом при измерениях. Поэтому для платины с зарядом 78 результат должен был быть меньше полученного, или другими словами у атома платины заряд ядра больше 78 и равен 82.
Построим модель ядра атома. Знаем что в ядре находятся протоны и нейтроны. В каждом последующем элементе на протон больше, а нейтронов на несколько. Почему? Обьем растет быстрее чем поверхность. При альфа излучении из ядра вылетают ядра гелия примерно одинаковых энергий. Разместив ядра гелия на поверхности ядра атома, получаем с некоторой точностью, что остальные нейтроны находятся внутри ядра. И вопрос а может ли и когда находится внутри ядра протон? Протоны, наверное, начинают размещаться внутри ядра с 72 по 75 элемент, а также со 108 по 111. Пока не открытые элементы.
Периодический закон принадлежит не только в химии, но и в физике.
Прошу повторить опыт Джеймса Чедвика по измерению заряда ядра атома платины. Заряды ядер меди и серебра сомнению не подлежат. Но согласно этой таблице элементов построенной как по закону Менделеева а также по правилу ван-Брука начиная с гафния заряды ядер могут быть на 4 единицы больше чем принято на сегодня при той же массе. Для задания режимов на АЭС, наверное важно знать истинный заряд ядра урана.
Дмитрий Иванович интуитивно чувствовал, что должна быть таблица элементов, а не сложная конструкция, как у него, но ему наверное не хватило знаний по устройству атома и ядра атома. Поэтому лантаноиды и актиноиды у него расположены горизонтально.
таблица элементов, физическая
| H 1 | He 2 | Li 3 | Be 4 | B 5 | C 6 | N 7 | O 8 | F 9 | Ne 10 | Na 11 | Mg 12 | Al 13 | Si 14 | P1 5 | S 16 | Cl 17 | A 1 | |
| K 19 | Ca 20 | Sc 21 | Ti 22 | V 23 | Cr 24 | Mn 25 | Fe 26 | Co 27 | Ni 28 | Cu 29 | Zn 30 | Ga 31 | Ge 32 | As 33 | Se 34 | Br 35 | Kr 36 | |
| Rb 37 | Sr 38 | Y 39 | Zr 40 | Nb 41 | Mo 42 | Tc 43 | Ru 44 | Rh 45 | Pd 46 | Ag 47 | Cd 48 | In 49 | Sn 50 | Sb 51 | Te 52 | I 53 | Xe 54 | |
| Cs 55 | Ba 56 | La 57 | Ce 58 | Pr 59 | Nd 60 | Pm 61 | Sm 62 | Eu 63 | Gd 64 | Tb 65 | Dy 66 | Ho 67 | Er 68 | Tu 69 | Yb 70 | Lu 71 | ? 72 | |
| ? 73 | ? 74 | ? 75 | Hf 76 | Ta 77 | W 78 | Re 79 | Os 80 | Ir 81 | Pt 82 | Au 83 | Hg 84 | Tl 85 | Pb 86 | Bi 87 | Po 88 | At 89 | Rn 90 | |
| Fr 91 | Ra 92 | Ac 93 | Th 94 | Pa 95 | U 96 | Np 97 | Pu 98 | Am 99 | Cm 100 | Bk 101 | Cf 102 | Es 103 | Fm 104 | Md 105 | No 106 | Lr 107 | ||
В квантовой механике
В
квантовой механике по умолчанию в каждом последующем элементе заряд
ядра увеличивается в его центре на единицу и идет заполнение электронами
spdf-конфигураций. У нас заряд ядра расположен на поверхности, т.к.
число протонов и число нейтронов в ядре таковы, что на поверхности ядра
должны быть протоны и нейтроны ,а внутри только нейтроны, то есть на
поверхности ядра образуется некая оболочка. Кроме того протоны должны
отталкиваться, а также их притягивает электронная шуба. Вопрос можно ли
считать в расчетах ядро точкой и до каких пор?
Литература
1. Г. Г. Филипенко. «Подозрительные» области в
периодической системе, "Техника и наука", №4,
Москва, 1990.
2. Г. Г. Филипенко. Предлагается модель ядра атома,
"Инженер", №4, Москва, 1991.
1. Г. Г. Филипенко. «Подозрительные» области в
периодической системе, "Техника и наука", №4,
Москва, 1990.
2. Г. Г. Филипенко. Предлагается модель ядра атома,
"Инженер", №4, Москва, 1991.
Sunday, June 1, 2014
1989г. Гродно.


https://natureofchemicalelements.blogspot.com
ReplyDeleteЗонная теория металла со стороны его кристаллической решетки.
ReplyDeletehttps://zen.yandex.ru/media/id/5ff97bc2aed88a7c9be811b5/zonnaia-teoriia-metalla-so-storony-ego-kristallicheskoi-reshetki-61bf253a33a97442c989209f